Maladies héréditaires
Les maladies génétiques sont dues à la présence d'anomalies chromosomiques ou de gènes mutants à hérédité particulière. De plus, des facteurs génétiques jouent un rôle dans la vulnérabilité à certaines MALADIES non héréditaires. En raison des progrès réalisés pour éliminer les maladies infectieuses, les maladies héréditaires en sont venues à représenter une proportion de plus en plus grande de l'ensemble des maladies. Celles des animaux, surtout des espèces domestiques, ont quelquefois apporté des renseignements utiles sur les affections qui leur correspondent chez les humains.
Au Canada, les premières études sur les maladies génétiques humaines ont été réalisées par Norma Ford WALKER (Toronto), Madge Macklin (London, Ontario) et F. Clarke FRASER (Montréal). Les progrès effectués récemment dans l'étude de l'ADN, base chimique des gènes, permettent désormais de déterminer le facteur principal de nombreuses maladies; ils laissent entrevoir la possibilité de comprendre les maladies héréditaires humaines et de les contrôler.
Si l'on connaît parfaitement une maladie sur le plan des gènes, on pourra peut-être remplacer les gènes défectueux grâce aux techniques du GÉNIE GÉNÉTIQUE. Les services de conseil génétique associés aux écoles de médecine et aux hôpitaux affiliés recueillent des données sur certaines maladies. Il est possible d'effectuer pour un certain nombre d'affections d'origine génétique des tests prénataux, qui font souvent appel à la technologie de l'ADN.
Aberrations chromosomiques
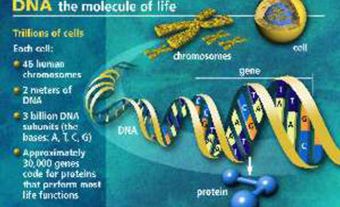
Les êtres humains possèdent 46 chromosomes, c'est-à-dire 22 paires d'autosomes plus deux chromosomes sexuels, responsables entre autres caractères, de la reproduction (XX chez la femme, XY chez l'homme). Tout matériel génétique surnuméraire ou déficitaire entraîne habituellement un arrêt de grossesse. Environ 15 p. 100 des grossesses se terminent par un avortement spontané (fausse couche) au cours des trois premiers mois; 40 à 50 p. 100 des foetus avortés présentent une aberration chromosomique.
Le type le plus commun d'aberration chromosomique chez les enfants nés vivants est le syndrome de Down, aussi appelé trisomie 21; les personnes atteintes ont 3 chromosomes 21 (au lieu de 2). L'incidence est d'environ 1 cas pour 700 grossesses (1 cas pour environ 40 chez les mères âgées de plus de 40 ans). Les sujets atteints présentent de multiples anomalies physiques et une déficience intellectuelle.
Les anomalies qui touchent un chromosome sexuel sont habituellement moins graves que celles des autosomes. L'absence d'un chromosome X entraîne le syndrome de Turner, présent chez environ 20 p. 100 de tous les foetus avortés spontanément et 0,0005 p. 100 des nouveau-nés; les sujets atteints présentent un développement mental normal, sont de petite taille et sont stériles. Les individus atteints du syndrome de Klinefelter (XXY) sont grands, souvent mentalement arriérés et possèdent des caractères sexuels secondaires peu développés. Les aberrations chromosomiques sont rarement héréditaires.
Maladies déterminés par un seul gène
La plupart des maladies héréditaires résultent de la transmission d'un seul gène fautif.
Maladies multifactorielles
Un grand nombre des anomalies congénitales (c'est-à-dire présentes à la naissance) les plus courantes sont des caractères multifactoriels causés par des facteurs environnementaux et génétiques. Parmi les anomalies de ce type, il faut citer le bec-de-lièvre et la fissure palatine, la sténose du pylore (occlusion de l'estomac) et les malformations du tube neural (spina bifida et anencéphalie). Son risque d'apparition chez les frères, les soeurs ou les descendants est d'environ 3 à 5 p. 100 selon le sexe de l'enfant atteint. On peut détecter les malformations du tube neural avant la naissance.
Les facteurs génétiques et environnementaux spécifiques de la plupart de ces anomalies n'ont pas encore été déterminés, mais on sait que la spécificité individuelle des antigènes HLA (c'est-à-dire les marqueurs situés à la surface des leucocytes humains), qui peuvent maintenant être identifiés grâce à la technologie de l'ADN, influent sur la vulnérabilité aux maladies associées au système immunitaire.
DIANE WILSON COX
Mécanismes moléculaires des maladies humaines
Nos connaissances des maladies humaines ont progressé rapidement grâce aux techniques de l'ADN recombinant (voir GÉNÉTIQUE). Des fragments d'ADN prélevés au hasard et qui présentent une variabilité élevée d'un individu à l'autre ont été utiles pour la cartographie génique des maladies humaines, en particulier les fragments d'ADN appelés microsatellites. Il s'agit de longues chaînes de séquences de bases répétitives que l'on trouve à de fréquents intervalles le long des chromosomes humains. Ils permettent de repérer l'emplacement des gènes.
Les laboratoires canadiens ont été particulièrement actifs dans le clonage des gènes en localisant leur position sur le chromosome. Parmi ces gènes, on peut citer celui de la dystrophie musculaire sur le chromosome X (Ronald Worton), de la mucoviscidose (Lap-Chee TSUI), de la tumeur de Wilms (Brian Williams), de l'anémie de Fanconi (Manuel Buchwald) et de la maladie de Wilson (Diane Cox).
Dès que le gène déterminant une maladie est identifié, on peut déterminer les changements spécifiques ou les mutations responsables de la maladie. Dès avant le clonage du gène, on peut repérer le gène dans la famille grâce aux marqueurs proches du gène afin d'établir le diagnostic de personnes présymptomatiques. Cette méthode sert actuellement pour de nombreuses maladies comme la chorée de Huntington et le rein polykystique.
Le Projet génome humain, dont le but est de séquencer le patrimoine génétique humain, a déjà fourni de précieuses renseignements sur le site des marqueurs et des gènes. À mesure qu'il progressera, les gènes normaux seront de plus en plus nombreux à être identifiés et cartographiés. La recherche de gènes responsables de maladies sera beaucoup plus facile, car on disposera de gènes candidats quand on connaîtra la position d'une maladie sur un chromosome. Il faut s'attendre à voir encore des progrès rapides dans la connaissance des maladies héréditaires humaines.
ROSE TEMPLETON
Auteurs ayant contribué à cet article:
Hérédité autosomique récessive
La maladie est transmise selon le mode récessif quand un caractère cliniquement reconnu est masqué chez les hétérozygotes, c'est-à-dire les individus qui ont hérité du gène de la maladie d'un seul parent. Seuls les homozygotes, c'est-à-dire les individus qui ont reçu le gène de la maladie de chaque parent, sont cliniquement atteints. On trouve fréquemment des anomalies partielles chez les hétérozygotes. Souvent, le gène en question produit normalement une enzyme qui est absente chez l'homozygote atteint. Ces anomalies enzymatiques, appelées erreurs innées du métabolisme, peuvent se manifester selon différentes voies biochimiques.
Normalement, certaines maladies génétiques se rencontrent dans tous les groupes raciaux, mais leur fréquence varie beaucoup d'un groupe racial à l'autre. La mucoviscidose constitue la maladie autosomique récessive la plus commune chez les enfants blancs. Les individus atteints présentent une anomalie de la sécrétion des enzymes du pancréas et du tube digestif. Un mucus visqueux peut provoquer l'occlusion des petits conduits aériens du poumon. La phénylcétonurie est due à un trouble du métabolisme d'un acide aminé, la phénylalanine (présente dans le lait), en raison de l'absence d'un enzyme chez les enfants atteints. Il en résulte une accumulation de produits toxiques anormaux qui entraînent un retard mental. De nombreuses provinces offrent des tests de dépistage pour déceler les sujets atteints (environ 1 nouveau-né pour 1000) et leur fournir immédiatement un régime pauvre en phénylalanine.
La maladie de Tay-Sachs est plus fréquente (1 cas pour 1600 naissances) chez les Juifs de souche ashkénaze que chez tout autre groupe racial. Un déficit enzymatique conduit à une détérioration neurologique et éventuellement à la mort (entre l'âge de deux et quatre ans). Il existe des anémies transmises selon le mode récessif qui peuvent être dues à une hémoglobine anormale. L'hémoglobine S, le type anormal le plus courant, cause la drépanocytose chez les homozygotes. Environ 1 noir américain sur 400 en est atteint. Les individus atteints souffrent d'une anémie grave et d'affections articulaires et musculaires de type arthritique.
Hérédité autosomique dominante
Les hommes comme les femmes peuvent présenter des signes cliniques de maladie s'ils sont porteurs d'un gène normal et d'un gène pathogène. Les individus atteints transmettent la maladie à 50 p. 100 de leurs descendants. Normalement, les maladies transmises selon le mode dominant ont une pénétrance variable, c'est-à-dire que certains sujets sont gravement atteints alors que d'autres présentent peu ou pas d'effets. La pénétrance variable est caractéristique dans l'ostéogenèse imparfaite qui se traduit par une fragilité osseuse anormale. La chorée de Huntington se caractérise par un âge d'apparition variable (à partir de 16 ans environ jusqu'à plus de 50 ans). Elle se manifeste par des mouvements brusques et saccadés des membres et une détérioration mentale.
Hérédité liée au chromosome X
Un gène déterminant une maladie, situé sur le chromosome X, peut être récessif ou dominant. Cependant, comme pour les caractères autosomes, le mode récessif est le plus courant. Ayant un gène normal sur l'un des deux chromosomes X, les femmes n'expriment pas la maladie tandis que les hommes sont atteints. Le meilleur exemple en est l'hémophilie, dont l'incidence chez l'homme est de 1 cas sur 10 000. La reine Victoria était porteuse de ce caractère, qui affecta certains de ses descendants mâles. La dystrophie musculaire, maladie musculaire dégénérative, d'évolution progressive, constitue un autre exemple de ce genre de maladie.

 Partager sur Facebook
Partager sur Facebook Partager sur X
Partager sur X Partager par Email
Partager par Email Partager sur Google Classroom
Partager sur Google Classroom